随着对心血管代谢疾病的认识不断深入,2型糖尿病(T2DM)管理格局进一步提升,提倡糖尿病与心肾疾病共管共治。在第61届欧洲糖尿病研究协会年会(EASD 2025)期间,针对T2DM心肾保护话题以及心血管-肾脏-代谢(CKM)综合征管理召开了多场研讨会。作为中国首个同时具有降糖、心血管和肾脏三大适应症的胰高糖素样肽-1受体激动剂(GLP-1RA),司美格鲁肽循证丰富,除改善代谢外,展现出的心肾获益“硬实力”令人瞩目!

紧随新理念:以患者为中心、心肾保护为导向,全面满足CKM治疗需求
糖尿病管理强调“以患者为中心”,从单纯的血糖控制,逐渐转向改善心肾结局与代谢控制并重的新理念。这一转变一方面基于糖尿病与心血管疾病、慢性肾脏病(CKD)之间相互纠缠、密不可分的关系,另一方面也得益于T2DM心肾保护治疗取得的重大进展。目前,国内外糖尿病指南一致强调,在控制血糖、控制危险因素的同时,应积极应用具有心肾保护证据的药物,如司美格鲁肽[1,2]。
这也成为EASD 2025会议的热点话题之一,在主题为“探索心血管代谢相关疾病以人为本的综合管理”的研讨会中,瑞典卡罗林斯卡大学医院Mikael Rydén教授特别展示了心血管代谢关键性结局方面的里程碑式证据(图1)[3]。其中,司美格鲁肽的循证获益证据丰富,广泛覆盖从血糖控制与体重管理,到心血管、肾脏、肝脏等整个疾病谱系,其证据之多、力度之强,在GLP-1类药物中令人深刻印象。
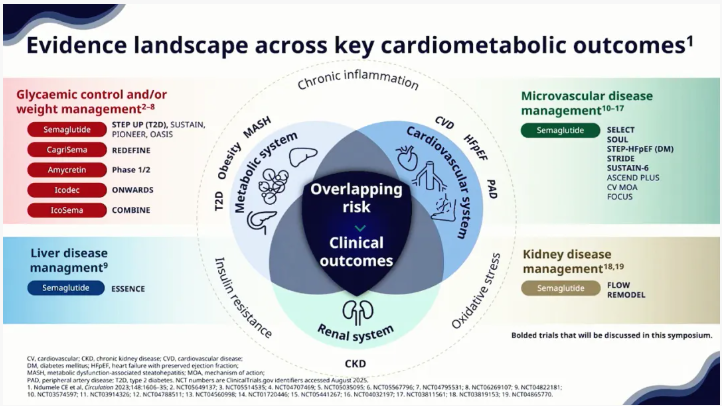
图1. 改善心血管代谢关键结局的里程碑证据

Steven Kahn教授
2025ADA班廷奖得主
华盛顿大学糖尿病研究中心
我认为司美格鲁肽在CKM管理中有着巨大潜力,我们应该了解当地监管机构批准司美格鲁肽的适应症,这对于临床获益的落地实践至关重要[4]。
血管保护:司美格鲁肽心血管获益优势凸显,超越减重的潜在机制有待深挖

John Buse教授
美国北卡罗来纳大学糖尿病中心
SUSTAIN 6、SOUL和SELECT研究结果高度一致,共同证实了不同剂型的司美格鲁肽分子均能改善心血管结局。其心血管获益的核心机制并非单纯依赖血糖或体重的改变,而是源于其多效性机制,包括抗炎、改善内皮功能以及稳定动脉斑块等直接血管作用[5]。
多项心血管结局研究(CVOT)和真实世界研究使得司美格鲁肽心血管获益形成完整证据链,无论注射液还是口服剂型,司美格鲁肽均显著降低主要心血管不良事件(MACE)风险。
SUSTAIN 6研究显示,在合并动脉粥样硬化性心血管疾病(ASCVD)或ASCVD高风险的T2DM患者中,司美格鲁肽0.5/1.0 mg注射液在标准治疗基础上,显著降低3P MACE(非致死性心肌梗死、非致死性卒中、心血管死亡)风险达26%,降低非致死性卒中风险达39%[6],还可降低主要冠脉事件(包括心肌梗死、冠脉血运重建)风险达26%[7]。在SOUL研究和SELECT研究中,口服司美格鲁肽片和司美格鲁肽注射液2.4 mg均能显著降低3P MACE风险[8,9],全面夯实了司美格鲁肽分子的心血管获益证据。
真实世界研究不仅进一步印证司美格鲁肽的心血管获益,还发现其降低MACE风险的能力较其他GLP-1类药物的优越性。REACH研究证实,在T2DM合并ASCVD的老年患者中,与度拉糖肽相比,司美格鲁肽显著降低3P MACE风险23%,显著降低5P MACE(卒中、心肌梗死、不稳定性心绞痛住院、心衰住院、全因死亡)25%(图2)[10]。

图2. REACH研究:司美格鲁肽降低MACE风险显著优于度拉糖肽
STEER研究证实,在超重或肥胖且已确诊心血管疾病但无糖尿病的患者中,司美格鲁肽2.4 mg降低MACE风险优于替尔泊肽,例如,在符合方案(PP)人群中,司美格鲁肽相较替尔泊肽显著降低心肌梗死、卒中以及心血管相关死亡或全因死亡风险达57%(图3)[11]。
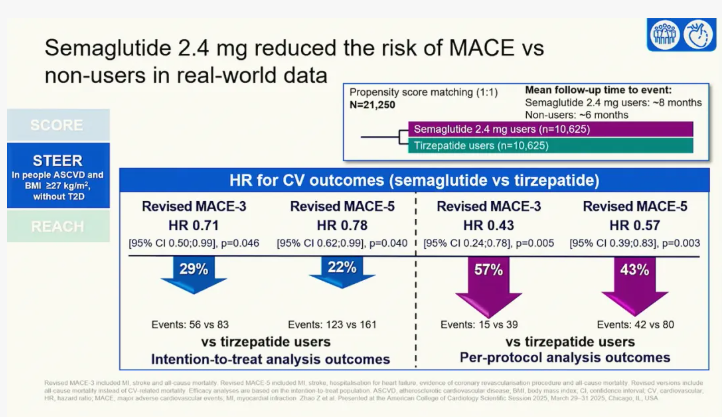
图3. STEER研究:司美格鲁肽降低MACE风险显著优于替尔泊肽
机制探索:司美格鲁肽心血管获益不主要依赖于减重,线粒体保护引关注
John Buse教授在演讲中特别强调,司美格鲁肽的心血管获益独立于基线BMI,无论是T2DM还是非糖尿病患者[5]。越来越多证据支持,尽管司美格鲁肽减重效果显著,但其心血管获益并不主要依赖于减重[6,12]。
目前认为,司美格鲁肽可能通过直接或间接等多种途径实现心血管获益,包括改善多重心血管代谢危险因素、直接作用于心脏和血管系统、发挥抗动脉粥样硬化作用等。其中,直接线粒体保护可能是其心血管获益的重要机制。高同源性的司美格鲁肽在体内的代谢产物如GLP-1(28-36)片段等可直接作用于线粒体,改善细胞能量代谢调节,进而产生更高的心血管保护效能[13]。
肾脏保护:司美格鲁肽是首个被证实肾脏获益的GLP-1RA类药物
在题为“关注肾脏——心血管代谢疾病中的协同策略”的主题发言中[14],Christoph Wanner教授指出T2DM合并CKD疾病负担沉重,并详细介绍了司美格鲁肽的肾脏获益证据及其可能机制。
肾脏结局研究力证:司美格鲁肽为T2DM合并CKD患者带来全面肾脏保护
以司美格鲁肽为代表的GLP-1RA的肾脏获益首先在CVOT研究中被发现,随后在肾脏结局研究(KOT)中被证实。FLOW研究是GLP-1RA类药物首个KOT研究,具有里程碑意义,其结果证实,T2DM合并CKD患者在标准治疗基础之上,应用司美格鲁肽注射液1.0 mg可进一步带来肾脏获益,包括降低主要肾脏复合事件风险达24%、降低尿白蛋白肌酐比值(UACR)达40%、显著延缓肾功能下降;同时可降低MACE风险18%,降低全因死亡风险20%[15]。

Christoph Wanner教授
德国维尔茨堡大学
在首个专门探索GLP-1RA肾脏结局的临床试验(FLOW)中,司美格鲁肽显著降低T2DM合并CKD患者发生肾脏事件的风险,且作用独立于体重减轻[14]。
此外,SELECT研究和SMART研究显示,在非糖尿病人群中,司美格鲁肽2.4 mg也展现出肾脏保护作用,包括改善蛋白尿、降低肾脏事件风险等[16,17]。这些证据进一步支持司美格鲁肽分子的肾脏获益。
机制探索:司美格鲁肽通过直接和间接作用共同保护肾脏
FLOW研究亚组分析表明,司美格鲁肽肾脏获益独立于基线体重指数(BMI),且不依赖于体重减轻[18]。目前认为,司美格鲁肽除通过改善多重代谢因素来保护肾脏外,还可直接作用于肾脏的GLP-1受体,通过抗炎、促进尿钠排出、抑制肾素-血管紧张素-醛固酮系统(RAAS)、改善血流动力学、改善内皮功能等机制,以预防和延缓CKD发生发展(图4)[19]。REMODEL 3期临床研究(NCT04865770)正在进行中,旨在探索司美格鲁肽在T2DM合并CKD患者中的肾脏保护机制,结果令人期待。
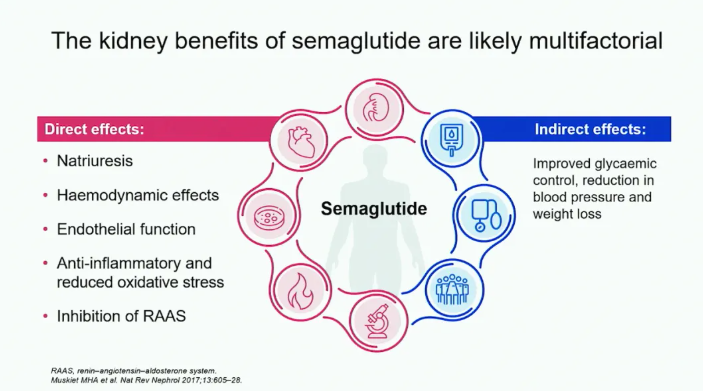
图4. 司美格鲁肽肾脏获益机制包括直接和间接作用
迈向下一步:司美格鲁肽有望成为T2DM合并CKD的第四大治疗支柱

Paola Fioretto教授
意大利帕多瓦大学
肾脏保护需要多靶点、多机制治疗,以更好地延缓肾病进展、改善心血管结局。司美格鲁肽有望成为T2DM合并CKD治疗的第四大支柱[20]。
T2DM合并CKD患者疾病负担沉重、预后较差而治疗手段相对较少,RAAS抑制剂(RAASi)、钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)和非甾体类盐皮质激素受体拮抗剂(nsMRA)是目前公认的三大治疗支柱,但患者仍有较高的心肾残留风险。2025美国糖尿病协会(ADA)《糖尿病医学诊疗标准》推荐具有明确肾脏获益的GLP-1RA作为T2DM合并CKD治疗的一线药物[1]。意大利帕多瓦大学Paola Fioretto教授在其报告[20]中表示,司美格鲁肽注射液在标准方案基础上进一步展现出显著肾脏获益,同时降低MACE风险和全因死亡风险,有望成为T2DM合并CKD的第四大治疗支柱,为进一步降低患者心肾风险提供更多选择(图5)[21]。

图5. 司美格鲁肽有望成为T2DM合并CKD的第四大治疗支柱
结语
目前,T2DM管理新理念强调以患者为中心,以心肾保护为导向,采取综合措施以更好地满足心血管代谢疾病治疗需求。具有明确心肾获益的GLP-1RA是指南推荐的一线药物,其中司美格鲁肽拥有丰富的循证医学证据,在改善代谢同时兼具心血管和肾脏获益,可为T2DM患者提供心肾代谢全面保护作用。近期,司美格鲁肽注射液新增CKD适应症,成为中国首个同时具有降糖、心血管和肾脏三大适应症的GLP-1RA,临床前景广阔。
司美格鲁肽凭借基于循证获益的“硬实力”,全面、全程覆盖CKM管理,在心血管代谢疾病中将发挥重要作用。期待其在临床实践中能得到合理积极应用,为广泛T2DM患者带来更多福祉!
参考文献
1. ADA. Diabetes Care. 2025; 48(Suppl 1): S1-S352.
2. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
3. Chairs: Alice Cheng, Mikael Rydén. Revolutionising cardiometabolic health: innovating, transforming and progressing care. Part 1: Exploring the background of person-centred care across the spectrum of related cardiometabolic diseases. Symposium at EASD 2025 meeting. MONDAY, 15 September 2025.
4. Steven Kahn. Chair. The Evolving Role of GLP-1RAs For Holistic Cardiovascular, Kidney, Liver and Metabolic Care. Symposium at EASD 2025 meeting. WEDNESDAY, 17 September 2025.
5. John Buse. Person-centred care – the need for treatment of cardiometabolic diseases. Presented at Symposium at EASD 2025 meeting. MONDAY, 15 September 2025.
6. Marso SP, et al. N Engl J Med. 2016; 375(19): 1834-1844.
7. Kolkailah AA, et al. Diabetes Obes Metab. 2023; 25(4): 1117-1120.
8. McGuire DK, et al. N Engl J Med. 2025; 392(20): 2001-2012.
9. Lincoff AM, et al. N Engl J Med. 2023; 389(24): 2221-2232.
10. Tan X, et al. Comparative effectiveness of once-weekly semaglutide vs dulaglutide on cardiovascular outcomes in US Medicare beneficiaries with type 2 diabetes and atherosclerotic cardiovascular disease. Presented at EASD 2025 meeting. LBA 19.
11. Wilson L, et al. Semaglutide is associated with lower risk of cardiovascular events compared with tirzepatide in patients with overweight or obesity and ASCVD and without diabetes in routine clinical practice. Presented at ESC 2025 meeting.
12. Zhou J, et al. Diabetes Obes Metab. 2025; 27(10): 5706-5715.
13. Tian MY, et al. Acta Pharmacol Sin. 2025; 46(5): 1250-1261.
14. Christoph Wanner. Focus on kidneys – synergistic strategies across cardiometabolic diseases. Presented at Symposium at EASD 2025 meeting. MONDAY, 15 September 2025.
15. Perkovic V, et al. N Engl J Med. 2024; 391(2): 109-121.
16. Colhoun HM, et al. Nat Med. 2024; 30(7): 2058-2066.
17. Apperloo EM, et al. Nat Med. 2025; 31(1): 278-285.
18. Mann JM, et al. Diabetes. 2025; 74(Suppl 1): 1971-LB.
19. Muskiet MHA, et al. Net Rev Nephrol. 2017; 13(10): 605-628.
20. Paola Fioretto. Taking the next step: the role of GLP-1RAs in the CKD and T2D nexus. Presented at Symposium at EASD 2025 meeting. WEDNESDAY, 17 September 2025.
21. Herrington WG, et al. N Engl J Med. 2024; 391(2): 178-179.
2 comments

紧随新理念:以患者为中心、心肾保护为导向,全面满足CKM治疗需求
糖尿病管理强调“以患者为中心”,从单纯的血糖控制,逐渐转向改善心肾结局与代谢控制并重的新理念。这一转变一方面基于糖尿病与心血管疾病、慢性肾脏病(CKD)之间相互纠缠、密不可分的关系,另一方面也得益于T2DM心肾保护治疗取得的重大进展。目前,国内外糖尿病指南一致强调,在控制血糖、控制危险因素的同时,应积极应用具有心肾保护证据的药物,如司美格鲁肽[1,2]。
这也成为EASD 2025会议的热点话题之一,在主题为“探索心血管代谢相关疾病以人为本的综合管理”的研讨会中,瑞典卡罗林斯卡大学医院Mikael Rydén教授特别展示了心血管代谢关键性结局方面的里程碑式证据(图1)[3]。其中,司美格鲁肽的循证获益证据丰富,广泛覆盖从血糖控制与体重管理,到心血管、肾脏、肝脏等整个疾病谱系,其证据之多、力度之强,在GLP-1类药物中令人深刻印象。

图1. 改善心血管代谢关键结局的里程碑证据

Steven Kahn教授
2025ADA班廷奖得主
华盛顿大学糖尿病研究中心
我认为司美格鲁肽在CKM管理中有着巨大潜力,我们应该了解当地监管机构批准司美格鲁肽的适应症,这对于临床获益的落地实践至关重要[4]。
血管保护:司美格鲁肽心血管获益优势凸显,超越减重的潜在机制有待深挖

John Buse教授
美国北卡罗来纳大学糖尿病中心
SUSTAIN 6、SOUL和SELECT研究结果高度一致,共同证实了不同剂型的司美格鲁肽分子均能改善心血管结局。其心血管获益的核心机制并非单纯依赖血糖或体重的改变,而是源于其多效性机制,包括抗炎、改善内皮功能以及稳定动脉斑块等直接血管作用[5]。
多项心血管结局研究(CVOT)和真实世界研究使得司美格鲁肽心血管获益形成完整证据链,无论注射液还是口服剂型,司美格鲁肽均显著降低主要心血管不良事件(MACE)风险。
SUSTAIN 6研究显示,在合并动脉粥样硬化性心血管疾病(ASCVD)或ASCVD高风险的T2DM患者中,司美格鲁肽0.5/1.0 mg注射液在标准治疗基础上,显著降低3P MACE(非致死性心肌梗死、非致死性卒中、心血管死亡)风险达26%,降低非致死性卒中风险达39%[6],还可降低主要冠脉事件(包括心肌梗死、冠脉血运重建)风险达26%[7]。在SOUL研究和SELECT研究中,口服司美格鲁肽片和司美格鲁肽注射液2.4 mg均能显著降低3P MACE风险[8,9],全面夯实了司美格鲁肽分子的心血管获益证据。
真实世界研究不仅进一步印证司美格鲁肽的心血管获益,还发现其降低MACE风险的能力较其他GLP-1类药物的优越性。REACH研究证实,在T2DM合并ASCVD的老年患者中,与度拉糖肽相比,司美格鲁肽显著降低3P MACE风险23%,显著降低5P MACE(卒中、心肌梗死、不稳定性心绞痛住院、心衰住院、全因死亡)25%(图2)[10]。

图2. REACH研究:司美格鲁肽降低MACE风险显著优于度拉糖肽
STEER研究证实,在超重或肥胖且已确诊心血管疾病但无糖尿病的患者中,司美格鲁肽2.4 mg降低MACE风险优于替尔泊肽,例如,在符合方案(PP)人群中,司美格鲁肽相较替尔泊肽显著降低心肌梗死、卒中以及心血管相关死亡或全因死亡风险达57%(图3)[11]。

图3. STEER研究:司美格鲁肽降低MACE风险显著优于替尔泊肽
机制探索:司美格鲁肽心血管获益不主要依赖于减重,线粒体保护引关注
John Buse教授在演讲中特别强调,司美格鲁肽的心血管获益独立于基线BMI,无论是T2DM还是非糖尿病患者[5]。越来越多证据支持,尽管司美格鲁肽减重效果显著,但其心血管获益并不主要依赖于减重[6,12]。
目前认为,司美格鲁肽可能通过直接或间接等多种途径实现心血管获益,包括改善多重心血管代谢危险因素、直接作用于心脏和血管系统、发挥抗动脉粥样硬化作用等。其中,直接线粒体保护可能是其心血管获益的重要机制。高同源性的司美格鲁肽在体内的代谢产物如GLP-1(28-36)片段等可直接作用于线粒体,改善细胞能量代谢调节,进而产生更高的心血管保护效能[13]。
肾脏保护:司美格鲁肽是首个被证实肾脏获益的GLP-1RA类药物
在题为“关注肾脏——心血管代谢疾病中的协同策略”的主题发言中[14],Christoph Wanner教授指出T2DM合并CKD疾病负担沉重,并详细介绍了司美格鲁肽的肾脏获益证据及其可能机制。
肾脏结局研究力证:司美格鲁肽为T2DM合并CKD患者带来全面肾脏保护
以司美格鲁肽为代表的GLP-1RA的肾脏获益首先在CVOT研究中被发现,随后在肾脏结局研究(KOT)中被证实。FLOW研究是GLP-1RA类药物首个KOT研究,具有里程碑意义,其结果证实,T2DM合并CKD患者在标准治疗基础之上,应用司美格鲁肽注射液1.0 mg可进一步带来肾脏获益,包括降低主要肾脏复合事件风险达24%、降低尿白蛋白肌酐比值(UACR)达40%、显著延缓肾功能下降;同时可降低MACE风险18%,降低全因死亡风险20%[15]。

Christoph Wanner教授
德国维尔茨堡大学
在首个专门探索GLP-1RA肾脏结局的临床试验(FLOW)中,司美格鲁肽显著降低T2DM合并CKD患者发生肾脏事件的风险,且作用独立于体重减轻[14]。
此外,SELECT研究和SMART研究显示,在非糖尿病人群中,司美格鲁肽2.4 mg也展现出肾脏保护作用,包括改善蛋白尿、降低肾脏事件风险等[16,17]。这些证据进一步支持司美格鲁肽分子的肾脏获益。
机制探索:司美格鲁肽通过直接和间接作用共同保护肾脏
FLOW研究亚组分析表明,司美格鲁肽肾脏获益独立于基线体重指数(BMI),且不依赖于体重减轻[18]。目前认为,司美格鲁肽除通过改善多重代谢因素来保护肾脏外,还可直接作用于肾脏的GLP-1受体,通过抗炎、促进尿钠排出、抑制肾素-血管紧张素-醛固酮系统(RAAS)、改善血流动力学、改善内皮功能等机制,以预防和延缓CKD发生发展(图4)[19]。REMODEL 3期临床研究(NCT04865770)正在进行中,旨在探索司美格鲁肽在T2DM合并CKD患者中的肾脏保护机制,结果令人期待。

图4. 司美格鲁肽肾脏获益机制包括直接和间接作用
迈向下一步:司美格鲁肽有望成为T2DM合并CKD的第四大治疗支柱

Paola Fioretto教授
意大利帕多瓦大学
肾脏保护需要多靶点、多机制治疗,以更好地延缓肾病进展、改善心血管结局。司美格鲁肽有望成为T2DM合并CKD治疗的第四大支柱[20]。
T2DM合并CKD患者疾病负担沉重、预后较差而治疗手段相对较少,RAAS抑制剂(RAASi)、钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)和非甾体类盐皮质激素受体拮抗剂(nsMRA)是目前公认的三大治疗支柱,但患者仍有较高的心肾残留风险。2025美国糖尿病协会(ADA)《糖尿病医学诊疗标准》推荐具有明确肾脏获益的GLP-1RA作为T2DM合并CKD治疗的一线药物[1]。意大利帕多瓦大学Paola Fioretto教授在其报告[20]中表示,司美格鲁肽注射液在标准方案基础上进一步展现出显著肾脏获益,同时降低MACE风险和全因死亡风险,有望成为T2DM合并CKD的第四大治疗支柱,为进一步降低患者心肾风险提供更多选择(图5)[21]。

图5. 司美格鲁肽有望成为T2DM合并CKD的第四大治疗支柱
结语
目前,T2DM管理新理念强调以患者为中心,以心肾保护为导向,采取综合措施以更好地满足心血管代谢疾病治疗需求。具有明确心肾获益的GLP-1RA是指南推荐的一线药物,其中司美格鲁肽拥有丰富的循证医学证据,在改善代谢同时兼具心血管和肾脏获益,可为T2DM患者提供心肾代谢全面保护作用。近期,司美格鲁肽注射液新增CKD适应症,成为中国首个同时具有降糖、心血管和肾脏三大适应症的GLP-1RA,临床前景广阔。
司美格鲁肽凭借基于循证获益的“硬实力”,全面、全程覆盖CKM管理,在心血管代谢疾病中将发挥重要作用。期待其在临床实践中能得到合理积极应用,为广泛T2DM患者带来更多福祉!
参考文献
1. ADA. Diabetes Care. 2025; 48(Suppl 1): S1-S352.
2. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
3. Chairs: Alice Cheng, Mikael Rydén. Revolutionising cardiometabolic health: innovating, transforming and progressing care. Part 1: Exploring the background of person-centred care across the spectrum of related cardiometabolic diseases. Symposium at EASD 2025 meeting. MONDAY, 15 September 2025.
4. Steven Kahn. Chair. The Evolving Role of GLP-1RAs For Holistic Cardiovascular, Kidney, Liver and Metabolic Care. Symposium at EASD 2025 meeting. WEDNESDAY, 17 September 2025.
5. John Buse. Person-centred care – the need for treatment of cardiometabolic diseases. Presented at Symposium at EASD 2025 meeting. MONDAY, 15 September 2025.
6. Marso SP, et al. N Engl J Med. 2016; 375(19): 1834-1844.
7. Kolkailah AA, et al. Diabetes Obes Metab. 2023; 25(4): 1117-1120.
8. McGuire DK, et al. N Engl J Med. 2025; 392(20): 2001-2012.
9. Lincoff AM, et al. N Engl J Med. 2023; 389(24): 2221-2232.
10. Tan X, et al. Comparative effectiveness of once-weekly semaglutide vs dulaglutide on cardiovascular outcomes in US Medicare beneficiaries with type 2 diabetes and atherosclerotic cardiovascular disease. Presented at EASD 2025 meeting. LBA 19.
11. Wilson L, et al. Semaglutide is associated with lower risk of cardiovascular events compared with tirzepatide in patients with overweight or obesity and ASCVD and without diabetes in routine clinical practice. Presented at ESC 2025 meeting.
12. Zhou J, et al. Diabetes Obes Metab. 2025; 27(10): 5706-5715.
13. Tian MY, et al. Acta Pharmacol Sin. 2025; 46(5): 1250-1261.
14. Christoph Wanner. Focus on kidneys – synergistic strategies across cardiometabolic diseases. Presented at Symposium at EASD 2025 meeting. MONDAY, 15 September 2025.
15. Perkovic V, et al. N Engl J Med. 2024; 391(2): 109-121.
16. Colhoun HM, et al. Nat Med. 2024; 30(7): 2058-2066.
17. Apperloo EM, et al. Nat Med. 2025; 31(1): 278-285.
18. Mann JM, et al. Diabetes. 2025; 74(Suppl 1): 1971-LB.
19. Muskiet MHA, et al. Net Rev Nephrol. 2017; 13(10): 605-628.
20. Paola Fioretto. Taking the next step: the role of GLP-1RAs in the CKD and T2D nexus. Presented at Symposium at EASD 2025 meeting. WEDNESDAY, 17 September 2025.
21. Herrington WG, et al. N Engl J Med. 2024; 391(2): 178-179.
2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言